爱必信(上海)生物科技有限公司品牌商
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
告别免疫无效:蒙脱土口服疫苗突破结直肠癌黏膜免疫激活瓶颈
42 人阅读发布时间:2026-04-08 10:29
在全球癌症负担日益沉重的背景下,结直肠癌作为高发的黏膜肿瘤,其治疗一直面临着传统疫苗难以激活黏膜免疫的困境。近日,《美国化学会志》(J. Am. Chem. Soc.)发表了一项突破性研究,研究团队成功开发出基于富锰蒙脱土纳米片的口服肿瘤治疗疫苗(Mn-MMT@OVA),为结直肠癌免疫治疗开辟了新路径。Absin ELISA 试剂盒助力该研究,见证了黏膜免疫激活策略的重大突破。
文献标题:Montmorillonite-Based Oral Vaccine for Colorectal Cancer Immunotherapy through Mucosal Immune Activation
发表期刊:Journal of the American Chemical Society(IF 15.6)
DOI:10.1021/jacs.5c06776
使用 Absin 产品:Mouse IL-4 ELISA Kit(abs520003)、Mouse IL-10 ELISA Kit(abs520005)、Human/Mouse/Rat TGF-β1 ELISA Kit(abs552208)

一、研究背景:黏膜肿瘤治疗的 “痛点” 与口服疫苗的 “机遇”
黏膜肿瘤(如结直肠癌)起源于黏膜组织,占全球癌症负担的重要比例。人体黏膜免疫系统占全身免疫细胞的 80%,是抵御黏膜肿瘤的关键防线,但传统皮下或肌内注射疫苗因 “免疫 compartmentalization” 效应,难以激活黏膜免疫,导致临床疗效不佳。
口服疫苗虽能利用肠道黏膜这一最大免疫器官,且具备安全性高、患者依从性好等优势,但面临三大挑战:胃酸和消化酶易降解抗原、肠道表面积大导致疫苗稀释、肠道免疫耐受抑制免疫应答。如何突破这些瓶颈,成为口服肿瘤疫苗研发的核心命题。
二、研究思路:精准设计,让疫苗在肠道 “精准发力”
研究团队创新性地选择蒙脱土(MMT)作为载体,通过离子交换技术将锰离子(Mn²⁺)和肿瘤抗原(OVA)嵌入其层状结构中,构建 Mn-MMT@OVA 口服疫苗。其核心设计逻辑如下:
1. 载体选择:蒙脱土天然具备耐胃肠道恶劣环境、黏膜黏附性强的特性,可作为 “疫苗储库” 保护抗原不被降解,并在肠道黏膜表面富集;
2. 免疫激活:Mn²⁺作为 cGAS-STING 通路的高效激活剂,能打破肠道免疫耐受,促进树突状细胞(DCs)成熟和抗原呈递;
3. 黏膜归巢:口服疫苗激活的免疫细胞会被 “黏膜印记”,表达 α4β7、CCR9 等归巢受体,精准迁移至结肠黏膜肿瘤部位,实现靶向杀伤。
三、核心研究成果:全方位验证疫苗的抗癌潜力
1. 疫苗结构稳定,肠道黏膜靶向富集
研究通过透射电镜(TEM)、原子力显微镜(AFM)等表征证实,Mn-MMT@OVA 具有典型层状结构,平均尺寸 182 nm,层间距扩展至 3.36 nm,确保 OVA 和 Mn²⁺稳定负载(OVA 负载率 64.2 wt%,Mn²⁺负载率 7.15 wt%)。在模拟胃肠液中,疫苗能保持结构稳定,2 小时内仅释放约 20% 的抗原和 Mn²⁺,进入肠道后 48 小时累计释放率达 80%,避免了胃酸中 “暴释”(对应原文图 1、图 2)。
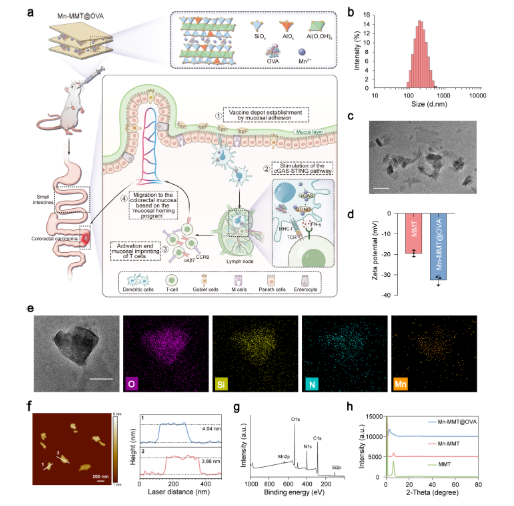
原文图1:Mn-MMT@OVA的合成与表征
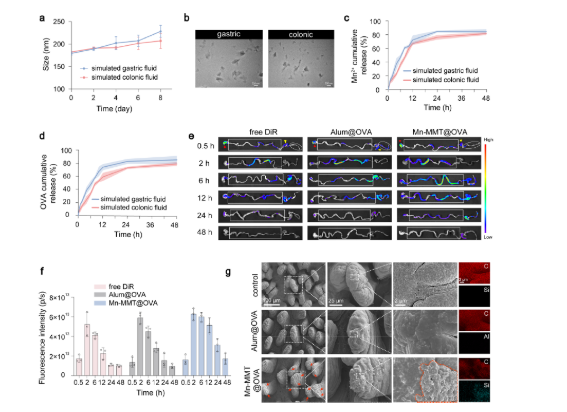
原文图2:Mn-MMT@OVA疫苗的黏膜黏附与储库建立
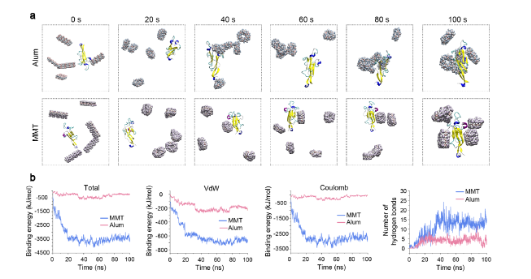
更重要的是,Mn-MMT@OVA 通过与肠道黏液蛋白(MUC2)的氢键、范德华力和静电作用,实现肠道黏膜高效黏附,形成 “疫苗储库”,显著延长肠道滞留时间(比传统铝佐剂疫苗长 2 倍以上)(对应原文图 2e-g、图 3)。
原文图3:MUC2与疫苗相互作用的分子动力学模拟
2. 高效激活 cGAS-STING 通路,打破免疫耐受
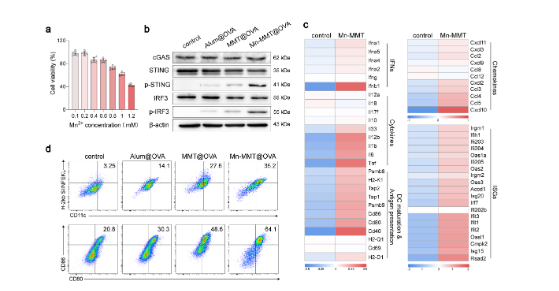
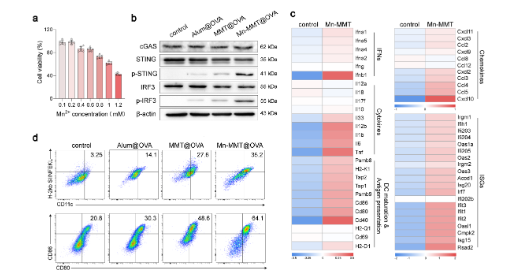
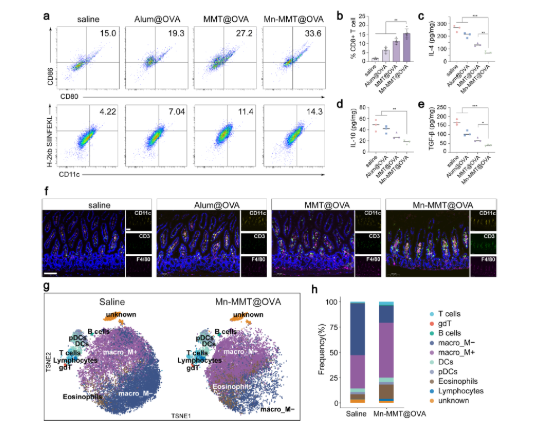
Mn-MMT@OVA 释放的 Mn²⁺能强效激活 DCs 中的 cGAS-STING 通路,使磷酸化 STING(p-STING)和磷酸化 IRF3(p-IRF3)表达显著升高,进而促进 DCs 成熟(CD11c⁺/CD80⁺/CD86⁺细胞比例达 64.1%)和抗原呈递(CD11c⁺/H-2Kb SIINFEKL⁺细胞比例达 86.0%),远优于传统铝佐剂疫苗(对应原文图 4a-d)。
原文图4:Mn-MMT@OVA对cGAS-STING通路的激活
3. 重塑肠道免疫微环境,强化抗肿瘤免疫
疫苗显著降低肠道内 IL-10、TGF-β 等抗炎因子水平,增加 CD8⁺ T 细胞比例,并促进巨噬细胞向 MHC-II⁺活化表型转化,形成促炎免疫微环境。CyTOF 分析显示,疫苗组肠道内 T 细胞、B 细胞、DCs 等免疫细胞亚群显著富集,为抗肿瘤免疫奠定基础(对应原文图 5)。
原文图5:肠道免疫微环境的调控
4. 显著抑制肿瘤生长,兼具黏膜与全身免疫应答
在结直肠癌原位模型中,口服 Mn-MMT@OVA 能显著抑制肿瘤生长,20 天后肿瘤重量较生理盐水组降低 70% 以上,肿瘤组织出现广泛坏死(对应原文图 6)。同时,疫苗诱导肠道黏膜产生高水平抗 OVA IgA(黏膜免疫标志)和血清 IgG(全身免疫标志),并促进 CD3⁺/α4β7⁺、CD3⁺/CCR9⁺归巢 T 细胞向肿瘤浸润,肿瘤内 CD8⁺ T 细胞比例达 8.03%,实现黏膜与全身免疫协同抗癌(对应原文图 7)。
原文图6:疫苗的体内抗肿瘤疗效
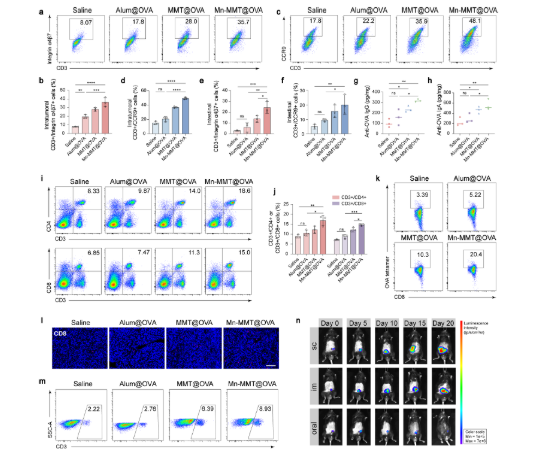
原文图7:黏膜和全身免疫应答的激活
5. 生物相容性优异,无明显毒副作用
实验期间小鼠体重稳定,心、肝、脾、肺、肾等重要器官无形态异常,血常规和肝肾功能指标均在正常范围,证实疫苗安全性良好(对应原文图 6f、图 S16-S17)。
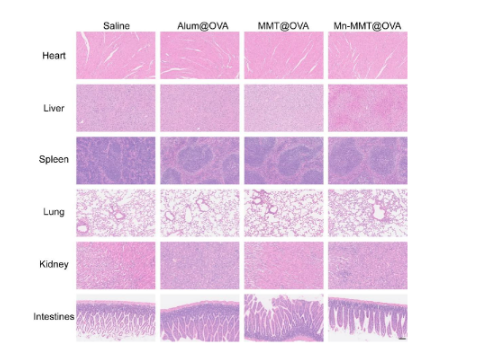
原文图S16:器官组织学分析
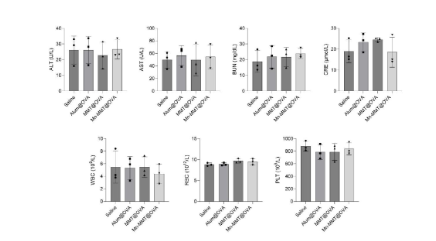
原文图S17:血常规和血清生化分析
四、Absin 产品助力:科研突破的 “关键工具支撑”
在这项高水平研究中,Absin 的核心产品为实验的顺利开展提供了关键保障,核心检测试剂盒精准量化肠道免疫微环境变化:
Mouse IL-4 ELISA Kit(abs520003):特异性检测小鼠肠道组织中 IL-4 的浓度水平,明确疫苗对 Th2 型免疫反应的调控作用,为评估肠道免疫微环境平衡提供直接数据。
Mouse IL-10 ELISA Kit(abs520005):精准定量肠道内 IL-10 的表达量,验证疫苗是否能有效降低抗炎因子水平,打破肠道免疫耐受(对应原文图 5d)。
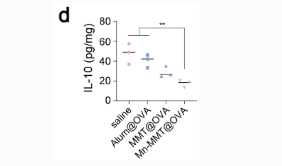
原文图5d:肠道IL-10水平检测(使用Absin Mouse IL-10 ELISA Kit)
Human/Mouse/Rat TGF-β1 ELISA Kit(abs552208):跨物种兼容的高灵敏度试剂盒,准确检测肠道组织中 TGF-β1 的含量变化,证实疫苗对免疫抑制性细胞因子的下调作用,为疫苗重塑肠道免疫微环境提供关键证据(对应原文图 5e)。
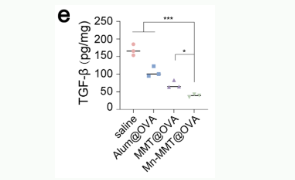
原文图5e:肠道TGF-β1水平检测(使用Absin Human/Mouse/Rat TGF-β1 ELISA Kit)
五、总结与展望
该研究创新性地将蒙脱土的黏膜黏附特性与 Mn²⁺的免疫激活功能相结合,构建了基于蒙脱土的口服结直肠癌疫苗,成功突破传统疫苗的黏膜免疫激活瓶颈。Absin 作为科研工具服务商,始终以高品质产品助力前沿科研,为肿瘤免疫治疗、纳米药物递送等领域的创新研究提供坚实支撑。
本文内容基于《Journal of the American Chemical Society》(DOI: 10.1021/jacs.5c06776)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。